Alcanos, alquenos, alquinos – es productos químicos orgánicos. Todos ellos están construidos de elementos químicos tales como el carbono y de hidrógeno. Alcanos, alquenos, alquinos – son compuestos químicos, que pertenecen al grupo de hidrocarburos.
En este artículo vamos a ver alquinos.
¿Qué es?
Estas sustancias también son llamados hidrocarburos de acetileno. La estructura del alquino proporciona la presencia en sus moléculas de hidrógeno y átomos de carbono. General de fórmula acetilénicos hidrocarburos tales: CnH2n-2. El más simple alquino sencilla – etino (acetileno). Tiene aquí una fórmula química – C 2 H 2. También se refiere a alquinos propino de la fórmula C 3 N 4. Además, para acetilénicos hidrocarburos pueden incluir butino (C 4 H 6), pentin (C 5 H 8) hexino (C 6 H 10) heptin (C 7 H 12), octino (C 8 H 14), nonino ( C 9 H 16) decino (C 10 H 18), y así sucesivamente. d. Todos los tipos de alquinos exhiben características similares. Vamos a examinar en detalle. 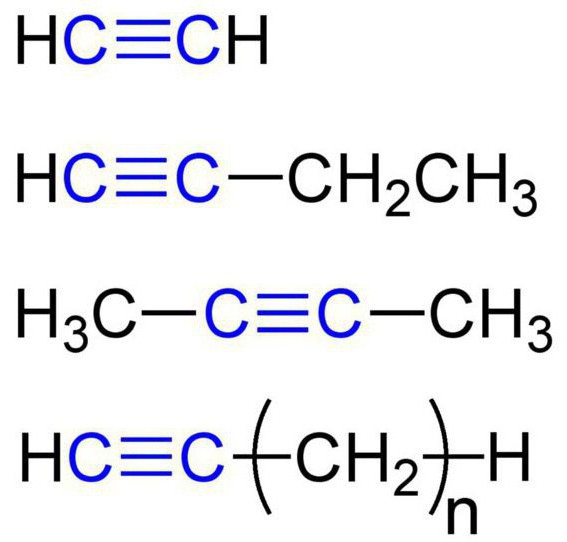
Las propiedades físicas de los alquinos
Las características físicas de los hidrocarburos de acetileno recuerdan alquenos.
En condiciones normales, alquinos, moléculas de los cuales contienen de dos a cuatro átomos de carbono, tienen un estado de agregación gaseoso. Esas moléculas de que es de cinco a 16 átomos de carbono, en condiciones normales de líquido. Los que están en las moléculas de los cuales 17 o más átomos de un elemento químico, – sólidos.
Los alquinos se funden y hierven a una temperatura mayor que los alcanos y alquenos.
Solubilidad en agua es insignificante, pero ligeramente superior a la de los alquenos y alcanos.
Solubilidad en disolventes orgánicos es alta.
El alquino más ampliamente usado – acetileno – tiene tales propiedades físicas:
- No tiene color;
- sin olor;
- en condiciones normales, está en un estado gaseoso de agregación;
- Tiene una densidad inferior a la del aire;
- punto de ebullición – menos 83,6 grados Celsius;
Las propiedades químicas de los alquinos
En estas sustancias, los átomos están unidos triple enlace, lo que explica sus propiedades básicas. Alquinos reaccionan este tipo:
- hidrogenación;
- gidrogalogenirovanie;
- halogenación;
- hidratación;
- quema.
Vamos a tomar con el fin. 
hidrogenación
Las propiedades químicas de los alquinos les permiten a participar en este tipo de reacción. Este tipo de interacciones químicas, en el que la molécula de la sustancia se adhiere a los átomos de hidrógeno adicionales. Este es un ejemplo de tal reacción química en el caso de propino:
2H 2 + C 3 H 4 = C 3 H 8
Esta reacción se produce en dos etapas. En la primera molécula de propino se une dos átomos de hidrógeno, y el segundo – la misma cantidad.
halogenación
Esta es otra reacción, que es parte de las propiedades químicas de los alquinos. Su molécula de hidrocarburo acetilénico resultado concede átomos de halógeno. Estos últimos incluyen elementos tales como cloro, bromo, yodo, etc.
Aquí está un ejemplo de una reacción de este tipo en el caso de etinil:
C 2 H 2 + 2SІ 2 = C 2 H 2 s² 4
El mismo proceso es también posible con otros hidrocarburos acetilénicos.
Gidrogalogenirovanie
También es una de las reacciones principales, que es parte de las propiedades químicas de los alquinos. Se encuentra en el hecho de que la sustancia se hace reaccionar con compuestos tales como NSІ, Ni, HBr, y otros. Esta reacción química se produce en dos etapas. Veamos la reacción de este tipo en el ejemplo de etinil:
C 2 H 2 + NSІ = C 2 H 3 s²
C 2 H 2 + s² NSІ = C 2 H 4 s² 2 
hidratación
Esta es una reacción química que está en contacto con agua. También se produce en dos etapas. Veamos en el ejemplo de etinil:
H 2 O + C 2 H 2 = C 2 H 3 OH
Una sustancia que se forma después de la reacción de la primera etapa llamada alcohol de vinilo.
Debido al hecho de que, según la regla de grupo funcional Eltekova OH no puede ser adyacente al doble enlace, el reordenamiento de los átomos, como resultado de lo cual el alcohol de vinilo se forma acetaldehído.
El proceso de la reacción de hidratación también llamado alquino Kucherova. 
ardiente
Este proceso de interacción de alquinos con el oxígeno a alta temperatura. Considere sustancias de este grupo quema con acetileno, por ejemplo:
2C 2 H 2 + 2O 2 = 2H 2 O + CO 2 + 3C
Cuando un exceso de oxígeno, acetileno y otros alquinos queman sin la formación de carbono. Por lo tanto asignado sólo monóxido de carbono y agua. Aquí está la ecuación de esta reacción con, por ejemplo propino:
4O 2 + C 3 H 4 = 2H 2 O + 3SO 2
La quema de otros hidrocarburos acetilénicos también ocurre de manera similar. Como resultado, se libera agua y dióxido de carbono.
otras reacciones
También acetilenos son capaces de reaccionar con las sales de metales tales como plata, cobre y calcio. Así, hay una sustitución de átomos de hidrógeno de metal. Considere este ejemplo en vista de la reacción con nitrato de acetileno y plata:
C 2 H 2 + 2AgNO3 = Ag 2 C 2 + 2NH 4 NO 3 + 2H 2 O
Otra interesante proceso que implica alquinos – reacción Zelinsky. Esta formación de benceno de acetileno cuando se calienta a 600 grados Celsius en presencia de carbón activado. La ecuación para esta reacción se puede expresar como sigue:
3C 2 H 2 = C 6 H 6
polimerización de alquinos como sea posible – el proceso de asociación de varias moléculas de la sustancia en un polímero. 
recepción
reacción alquino que hemos discutido anteriormente, se preparan en el laboratorio de varias maneras.
El primero – un deshidrohalogenación. Parece ecuación de reacción así:
C 2 H 4 Br 2 + 2KOH = C 2 H 2 + 2H 2 O + 2KBr
Para la realización de este proceso es calentar los reactivos, y añadir etanol como catalizador.
También existe la posibilidad de alquinos a partir de compuestos inorgánicos. He aquí un ejemplo:
CaC 2 + H 2 O = C 2 H 2 + 2CA (OH) 2
El siguiente método de producción de alquino – deshidrogenación. Este es un ejemplo de tal reacción:
= 3H 2 CH 4 + 2 C 2 H 2
Con este tipo de reacción se puede obtener no sólo etino, pero otros hidrocarburos acetilénicos.

El uso de alquino
El más ampliamente utilizado en la industria fue la más simple alquino – etino. Es ampliamente utilizado en la industria química.
- Se necesita alquinos de acetileno u otros para la producción de uno otros compuestos orgánicos tales como cetonas, aldehídos, y otros disolventes.
- También desde alquinos se pueden obtener sustancias que se usan en la fabricación de cauchos, cloruro de polivinilo y otros.
- De propino se puede obtener como un resultado acetona RAKTs Kucherova.
- Por otra parte, el acetileno se utiliza en la preparación de productos químicos tales como ácido acético, hidrocarburos aromáticos, alcohol etílico.
- Más acetileno se utiliza como un combustible con un alto calor de combustión.
- También reacción de combustión etinilo se usa para la soldadura de metales.
- Además, usando un acetileno puede prepararse de carbono Técnica.
- Además, esta sustancia se utiliza en aparatos independientes.
- El acetileno y otros hidrocarburos número de este grupo se utilizan como propelentes debido a su alto calor de combustión.
En esta aplicación alquinos termina. 
conclusión
A medida que la parte final de la tabla es un resumen de las propiedades de los hidrocarburos de acetileno y su preparación.
| Nombre reacciones | explicaciones | ejemplo ecuación |
| halogenación | reacción de adición de una molécula de los átomos de halógeno de hidrocarburos acetilénicos (bromo, yodo, cloro, etc.). | C 4 H 6 + 2I 2 = C 4 H 6 de I 2 |
| hidrogenación | reacción de adición de un alquino átomos de hidrógeno de la molécula. Se produce en dos etapas. |
C 3 H 4 + H 2 = C 3 H 6 C 3 H 6 + H 2 = C 3 H 8 |
| Gidrogalogenirovanie | reacción de adición de la gidrogalogenov hidrocarburo molécula de acetileno (ni, NSІ, HBr). Se produce en dos etapas. |
C 2 H 2 + ni = C 2 H 3 de I C 2 H 3 + ni de I = C 2 H 4 I 2 |
| hidratación | Las reacciones, que se basa en la interacción con el agua. Se produce en dos etapas. |
C 2 H 2 + H 2 O = C 2 H 3 OH C 2 H 3 OH = CH 3 -CHO |
| La oxidación completa (combustión) | Atsetilenovgo reaccionar hidrocarburo con oxígeno a una temperatura elevada. Esto produce monóxido de carbono y agua. |
2C 2 H 5 + 5O 2 = 2H 2 O + 4CO 2 2C 2 H 2 + 2O 2 = H 2 O + CO 2 + 3C |
| Las reacciones con sales de metales | Consiste en el hecho de que los átomos metálicos están sustituidos con átomos en las moléculas de hidrógeno hidrocarburos acetilénicos. |
C 2 H 2 + AgNO3 = C 2 Ag 2 + 2NH 4 NO 3 + 2H 2 O |
Obtener alquinos pueden estar en el laboratorio usando tres métodos:
- compuestos inorgánicos;
- por deshidrogenación de compuestos orgánicos;
- método deshidrohalogenación de sustancias orgánicas.
Así que miramos todas las características físicas y químicas del alquino, sus métodos de preparación, aplicaciones en la industria.


















