Tal vez, cada hogar tiene una cocina de soda – caja de aspecto corriente con una sustancia en polvo. culinaria anfitriona usarlo como aditivo para preparados para hornear. Sin embargo, su alcance es tan amplio que una sustancia seguridad se puede llamar persona asistente universal. Pero lo que es un refresco? ¿Qué tipo y la forma en que existe se utiliza en la vida cotidiana?

nombres de soda
Antes de proceder a las propiedades químicas de soda, vale la pena mencionar que su nombre – "Soda", una sustancia obtenida a partir del nombre de la planta saltwort sodonosnaya, ceniza, que es una fuente de producción de soda.
En química, soda – generaliza sales de sodio de título de ácido carbónico:
- Na 2 CO 3 (carbonato de sodio) – fórmula química de la ceniza de sosa;
- Na 2 CO 3 · 10H 2 O – soda de lavado;
- NaHCO3 – bicarbonato de sodio. Esta es la fórmula química de bicarbonato de sodio;
- Na 2 CO 3 · H 2 O o Na 2 CO 3 · 7H 2 O – fórmula química cristal soda.
En la vida cotidiana, así como hay varios tipos de material trivial en la industria química:
- bicarbonato de sodio;
- bicarbonato de sodio;
- bicarbonato de sodio;
- aditivo E500;
- decahidrato sódico.

La fórmula empírica
La fórmula química de bicarbonato de sodio – NaHCO3. Este ácida de sal de ácido carbónico. Si se suman los pesos atómicos de todos sus elementos constitutivos, resulta que el peso atómico del sodio es igual a 84 a. e.
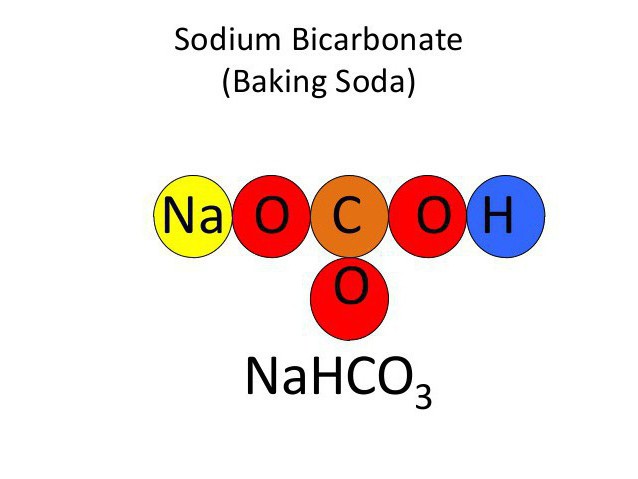
El método de su formación es bastante simple. La fórmula química de bicarbonato de sodio – una interacción compleja de hidróxido de sodio con ácido carbónico:
NaOH + H 2 CO 3 = NaHCO3 + H 2 O.
En química, sodio dvuuglikisly es un complejo de ácido de sodio anión carbonato y de cationes. Cuando la introducción de estos elementos en el cuerpo, que normalizan el equilibrio ácido-base neutralizando el ácido en exceso presente en el medio líquido.
carbonato de sodio
La fórmula química de la ceniza de sosa – Na2CO3. Soda Ash – es un material blanco, granular que se puede representar en la forma de gránulos (A) o en polvo (B).
Este tipo de ceniza tiene varias características que lo distinguen carbonato de sodio de los alimentos.
- pH del medio. Y la comida y ceniza de sosa – es alcalino, pero el primero – bajo, con pH = 8, y el segundo – alta, con pH = 11. La naturaleza del medio y la fórmula química indica sosa técnica.
- Ámbito de aplicación. El bicarbonato de sodio se utiliza en la cocina, cosméticos y medicamentos. Soda se utiliza como un agente de limpieza eficaz.
En el hogar utilizando carbonato de sodio puede ser:
- participado en el lavado, usándolo como un detergente de lavandería;
- lavar el piso, pero esta herramienta no es adecuada para laminado y suelo de parquet, ya que puede estropear el revestimiento;
- eliminar los bloqueos de tubería;
- artículos de limpieza de la porcelana.
Cuando se utiliza carbonato de sodio debe ser muy cuidadoso, ya sustancia altamente tóxica perteneciente al tercer grupo de agentes peligrosos.

Las propiedades físicas de bicarbonato de sodio
El bicarbonato de sodio es una sustancia en polvo de color blanco. Este complejo elementos de sodio, hidrógeno, carbono y oxígeno.
Por densidad de polvo igual a 2,16 g / cm 3.

Cuando el parámetro de temperatura de 50 -60 C. sustancia comienza a derretirse.
El bicarbonato de sodio, o bicarbonato de sodio está representado en la forma de leche en polvo. En el medio ambiente acuático perfectamente soluble. Que no se queme. La fórmula química de bicarbonato de sodio es el mismo que el de la comida.
solución de sosa

Bicarbonato de sodio – una sustancia que se disuelve completamente en agua, resultando en una solución de sosa. Se utiliza con fines de higiene como un enjuague bucal.
solución Fórmula química de sodio es la siguiente:
NaHCO3 + H 2 O = H 2 CO 3 + NaOH.
La solución acuosa de sosa dotado de carácter débilmente básico.
El sodio se disocia dvuuglikisly en solución acuosa para formar los siguientes iones:
Na 2 CO 3 ↔ 2Na + + CO3 2-
Propiedades de sodio como un álcali
Como se ha mencionado, el hidrógeno carbonato de sodio es una sustancia alcalina. Este hecho afecta el uso de bicarbonato de sodio como un medio para neutralizar la acidez del cuerpo, especialmente del estómago. Los elementos que componen la materia, tienen una exposición segura.
operabilidad Soda renal mejora porque derivable orina tiene un medio alcalino. Además, se mantiene la cantidad necesaria de AK glutámico en el cuerpo, lo que evita la aparición de formaciones de piedra en los riñones.
ambiente alcalino ayuda a una mejor digestión de ciertas vitaminas del grupo B: B1, B4, B5, B6 y B12.
Cuando refresco utilizada para la buena digestión combinarlo con leche caliente. Esto contribuye al hecho de que el pequeño sosa intestino reacciona con los aminoácidos de la leche, lo que podría dar lugar a la sal de sodio de aminoácidos que tiene una naturaleza alcalina. Estos aminoácidos son mucho mejores que las bebidas gaseosas, entrar en el torrente sanguíneo, lo que aumenta las reservas alcalinas del cuerpo.
sosa cáustica
La fórmula química de sosa cáustica – NaOH. Fórmula estructural: Na – O – H.
Las sustancias de peso molecular constituyen el peso atómico de sus componentes constituyentes Na, O y H. Es igual a 40.
Caustic perfectamente soluble en agua.
En la industria en relación con este tipo de refresco se utilizan los siguientes nombres:
- sosa cáustica;
- hidróxido de sodio;
- hidróxido de sodio.
Cuando se trabaja con sosa cáustica es necesario el uso de elementos de protección de la ropa, como en el contacto con la piel que deja quemaduras graves.
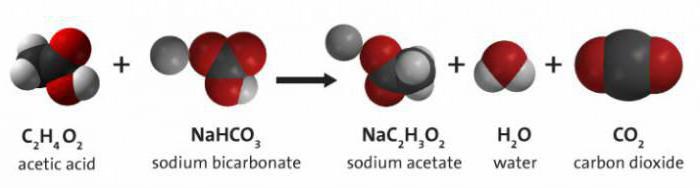
Soda en combinación con vinagre
Fórmula química vinagre y bicarbonato de sodio es una reacción de templado que produce agua, dióxido de carbono y sal de ácido acético.
Esta "experiencia" química viene acompañado de un silbido característico, que indica el comienzo de la "quema" de soda.
Esta reacción se lleva a cabo en el negocio culinario, cuando la intención de amasar la masa para hornear. Vinagre para esto se toma en una concentración de 9%. análogo del ácido puede ser un vinagre de jugo de limón, la sidra de manzana o vino.
Entonces, ¿por llevar a cabo la reacción en la preparación de la prueba? El caso es que como resultado de la descomposición de sosa dióxido de carbono da esplendor de prueba.
conseguir sustancia
Una vez extraído de ceniza de sosa plantas halófilas sodonosnoy. Actualmente, la base para la preparación de esta sustancia es un producto natural sulfato de sodio. Preparación de reacción es como sigue, donde el lado derecho se muestra la fórmula química de sosa:
Na 2 SO 4 + 3C + 2O 2 = 2Na 2 CO 3 + CO 2 + 2SO 2;
CaCO 3 + C + Na 2 SO 4 = Na 2 CO 3 + 4CO + CaS.
El uso de bicarbonato de sodio
Soda es muy popular en la vida cotidiana, no sólo como un componente culinaria. Sin embargo, una mirada más atenta a los casos en que se utiliza la ceniza.
- Para empezar es mencionar una vez más que la soda – componente de alimentos en el negocio culinario. Su uso no es al azar: calentando el compuesto capaz de liberar vapores de dióxido de carbono, que a su vez da ligereza prueba. En este caso, la soda actúa como disgregante. Pero si usted compra en una bolsa de la tienda con el polvo de hornear pasteles, a continuación, en el paquete en la línea puede detectar la presencia de sosa, que se designa como aditivo alimentario E500.
- Use bicarbonato de soda y bebidas gaseosas.
- Muy a menudo, la soda se utiliza en la llamada medicina "tradicional". En esta región, que sobresale cura sosa casi cualquier dolencias, por ejemplo, su eficacia se ha demostrado para la acidez estomacal, tos, dolor en la garganta, el estómago, a una temperatura elevada.
- Funcionado bien y bicarbonato de sodio como agente de limpieza. Puede ser utilizado para la limpieza de artículos sanitarios, las cacerolas de aluminio, platos, alfombras, plata y lavandería. La sustancia tiene un buen desinfectante y antifúngica.
- Muchas mujeres usan bicarbonato de soda para fines cosméticos y de higiene. Se puede utilizar como un exfoliante para la piel. Significa gran parada de la piel áspera pies si se utiliza para baños de pies. Se puede utilizar para deshacerse del olor a sudor en el área de la axila, o en el zapato.
Se ayuda a los dientes de soda y blanqueo. Esta es una forma barata pero efectiva. polvo de sodio se mezcla con pasta de dientes y agua o movimientos suaves realizados de limpieza de dientes.
La sosa cáustica: el uso
El uso de este tipo de refresco debe ir acompañada de ciertas medidas de seguridad como la soda cáustica – un álcali fuerte que puede "comer fuera" muchos tipos de superficies.
Lo que también puede ser útil en los términos de uso doméstico cáusticos?
- Cáustica hace frente a diferentes impurezas en los platos. Pero es necesario que se abstengan de la utilización de este agente para productos hechos de aluminio y teflón. Pero para el resto de las ollas, sartenes o bandejas para hornear – por favor. Nagar, escala, tapada capas de grasa – todo esto es fácil de manejar cáusticos.
- La sosa cáustica puede resolver el problema de las tuberías obstruidas. Sólo tiene que rellenar la sustancia granular en el tubo y dejar actuar durante un tiempo, luego enjuague con agua corriente.
La sosa cáustica, también conocido como sosa cáustica, es ampliamente aplicable a escala industrial en diversos campos de la producción.
- En la construcción. En este caso, la sustancia utilizada para hacer algunos tipos de materiales de construcción, y también sirve como un componente adicional que refuerza la base fundamental de las estructuras.
- En la industria alimentaria. La sosa cáustica es aplicable y alimentos de fabricación. Por supuesto, en este caso se utiliza en concentraciones bajas. Con su participación producir cacao en polvo, chocolate, helados, dulce de leche, en la cocción de pan, se utiliza como aditivo E524.
- industria textil. En esta área, la sosa cáustica es útil en el blanqueo de la tela y la regeneración de productos de caucho.
- Producción química: sosa cáustica se usa como neutralizadores de ácido, medios para la limpieza de aceite y los productos basados en él. La producción de aceites industriales también no puede prescindir de la adición de sosa cáustica. Además, hidróxido de sodio – un buen catalizador de algunas reacciones químicas.
- sosa cáustica adecuados para la fabricación de jabón y la fabricación de varios tipos de jabones, champús y geles.
La ceniza de sosa: uso
carbonato de sodio también se conoce como el lino. La demanda especial para esta instalación disfrutado en la Unión Soviética, por lo tanto, podemos decir: la soda de lavado es la prueba del tiempo.
Los medios empleados en las siguientes situaciones:
- Durante los artículos a lavar.
- Al limpiar las superficies de azulejos, gres, loza de barro.
- Al quitar una obstrucción en los tubos.
- Para eliminar la escoria en el tambor de una lavadora, así como en los platos.
- Para la destrucción de las plagas de insectos en los jardines.
A partir de lo anterior, la conclusión se sugiere: Soda herramienta versátil que se utiliza en la mayoría de las áreas de la vida, tanto doméstico como industrial.
El material de buena calidad es el hecho de que se puede comprar por algunos centavos.