Molecular y estructural fórmula metano
Fórmula molecular, estructural y electrónica de metano se basan en la teoría de la estructura de los compuestos orgánicos Butlerov. Antes de escribir estas fórmulas, comenzamos con una breve caracterización del hidrocarburo.

Características de metano
Esta sustancia es un explosivo, sino que también se llama de gas "pantano". El olor específico de los hidrocarburos limitantes conocido por todos. El proceso de combustión de la misma se dejó componentes químicos perjudiciales para el cuerpo humano. Que el metano es un participante activo en la formación del efecto invernadero.
propiedades físicas
El primer representante de la serie homóloga de alcanos ha sido descubierto por los científicos en la atmósfera de Titan y Marte. Teniendo en cuenta el hecho de que el metano está ligada a la existencia de organismos vivos apareció hipótesis de la existencia de vida en estos planetas. En Saturno, Júpiter, Neptuno, Urano, producto de metano apareció procesamiento como química de las sustancias de origen inorgánico. En la superficie de nuestro planeta a su bajo contenido.
características generales
El metano no tiene color, que es más ligero que el aire casi el doble, es poco soluble en agua. La composición de gas natural la cantidad alcanza el 98 por ciento. El gas aceite que pasa contiene de 30 a 90 por ciento de metano. En más metano es de origen biológico.
Ungulates herbívoros cabras y vacas emiten el procesamiento en los estómagos de bacterias cantidad bastante significativa de metano. Entre las fuentes importantes de la serie homóloga de alcanos seleccione pantanos, termitas, filtrando fotosíntesis de las plantas de gas natural. En la detección de trazas de metano en el planeta, podemos hablar de la existencia de su vida biológica.

Métodos para la preparación
La fórmula estructural detallado de metano es evidencia de que en su molécula única saturado enlaces simples formadas nubes híbridas. preparación realizaciones de laboratorio adicionales de la nota de hidrocarburo de aleación con acetato de sodio sólido con álcali, y la interacción de carburo de aluminio con agua.
Sólido metano llama azulada, destacando al mismo tiempo el orden de 39 MJ por metro cúbico. mezcla explosiva forma la sustancia al aire. El metano más peligroso, que se libera durante la minería subterránea de depósitos minerales en las minas de montaña. Alto riesgo de explosión de metano y plantas de beneficio de carbón y de fabricación de briquetas, así como las industrias de clasificación.
efecto fisiológico
Si el porcentaje de metano en el aire es de 5 a 16 por ciento, en contacto con el oxígeno puede ser encendido metano. En caso de un aumento significativo en la mezcla de la sustancia química aumenta la probabilidad de explosión.
Si la concentración de aire del alcano es 43 por ciento, es la causa asfixia.
Con la velocidad de propagación de la explosión de 500 a 700 metros por segundo. Una vez que el metano se pone en contacto con una fuente de calor, proceso de encendido alcano se produce con un cierto retraso.
Fue en esta producción basada en la propiedad de los equipos y la seguridad de los componentes explosivos eléctrica a prueba de explosiones.
Desde el metano es el hidrocarburo saturado más estable térmicamente, que es ampliamente utilizado como combustible industrial y doméstico y también se utiliza como una materia prima valiosa para la síntesis química. La fórmula estructural de etil-tri-metano caracteriza a las características estructurales de los miembros de esta clase de hidrocarburos.
En el proceso de reacción química con cloro por la exposición a la radiación ultravioleta puede estar formado por varios productos de reacción. Dependiendo de la cantidad de material de partida puede estar en la sustitución recibir clorometano, cloroformo, tetracloruro de carbono.
En el caso de una combustión incompleta del metano formado hollín. El formaldehído se forma en el caso de la oxidación catalítica. El producto de reacción final es disulfuro de carbono con azufre.

estructura de metano propiedades
¿Cuál es su fórmula estructural? El metano se refiere a hidrocarburos saturados que tienen la fórmula general C n H 2n + 2. Considere una formación molécula particular para explicar cómo se forma la fórmula estructural.
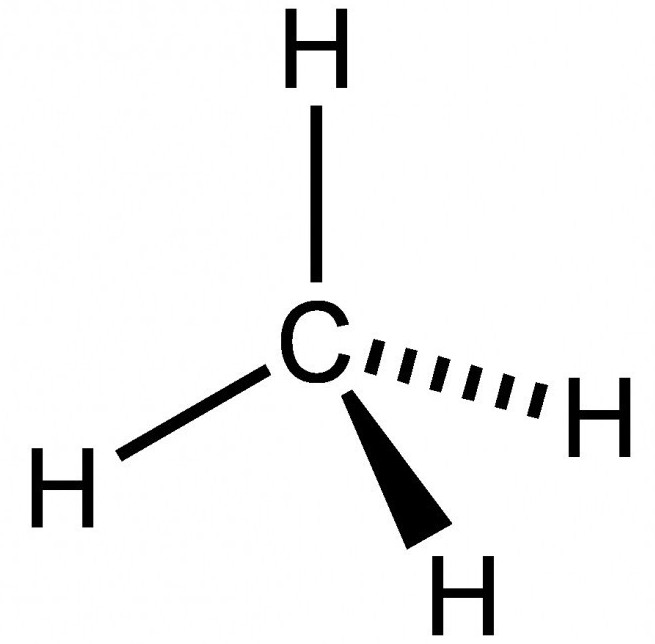
El metano se compone de un átomo de carbono y cuatro átomos de hidrógeno unidos por enlace covalente momento dipolar. Se explica la estructura basada en los átomos de carbono fórmulas estructurales.
Ver la hibridación
La estructura espacial de metano caracteriza por la estructura tetraédrica. Desde externamente en el carbono cuatro electrones de valencia, la transición de electrones se produce en el átomo de calefacción con un segundo s-orbitales p. Como resultado, el último nivel de potencia en el carbono se encuentra cuatro desapareado ( "libre") del electrón. fórmula estructural completa de metano se basa en el hecho de que la formación de los cuatro nubes híbridas que están orientados en el espacio en un ángulo de 109 grados 28 minutos, formando una estructura tetraedro. Además hay vértices superposición de nubes híbridas con átomos de nubes de hidrógeno no híbridos.
fórmula estructural completa y el metano condensado cumple plenamente teoría Butlerova. Entre sencilla enlace formas de carbono e hidrógeno (single), por lo que las reacciones químicas no son conexión típica.
A continuación se muestra la fórmula estructural final. El metano – es el primer representante de la clase de hidrocarburos saturados, que tiene las propiedades típicas limitan alcano. Fórmula estructural E y metano confirmar el tipo de hibridación de átomo de carbono en la materia orgánica.

Desde el curso de química de la escuela
Esta clase de hidrocarburos, representante de los cuales es un "gas de los pantanos", estudiada en el curso de 10 clases de la escuela secundaria. Por ejemplo, los niños propusieron la tarea de caracteres siguientes: "Escribir las fórmulas estructurales de metano". Se debe entender que sólo una configuración estructural detallada para esta sustancia, se puede pintar en la teoría Butlerova.
Su fórmula abreviada será el mismo que el molecular, escrita en forma de CH4. Bajo las nuevas normas federales de educación que se imponen en relación con la reorganización de la educación rusa en el curso básico de química todos los asuntos relativos a las características de las clases de sustancias orgánicas, comprenden la vigilancia.
síntesis industrial
procesos industriales a base de metano tal un componente químico importante se han desarrollado como acetileno. La base de craqueo térmico o eléctrico fue precisamente su fórmula estructural. El metano en la oxidación catalítica de amoníaco para formar ácido cianhídrico.
Aplicar este material orgánico para la producción de gas de síntesis. Por reacción con vapor, una mezcla de monóxido de carbono e hidrógeno, que son materias primas para el límite de la producción de alcoholes monovalentes, compuestos de carbonilo.
De particular importancia es la reacción con ácido nítrico, lo que resulta en nitrometano.

El uso como carburante
Debido a la falta de fuentes naturales de hidrocarburos, así como el empobrecimiento de la base de recursos, sobre todo asunto relevante relacionada con la búsqueda de nuevas fuentes (alternativos) de combustible. Una de ellas es el biodiesel, que incluía allí y metano.
Dada la diferencia de densidad entre el combustible de gasolina y el primer miembro de la clase de los alcanos, hay ciertas características en su aplicación como fuente de energía para los motores de automóviles. Con el fin de evitar la necesidad de llevar una gran cantidad de metano, por la compresión para aumentar su densidad (bajo una presión de aproximadamente 250 atmósferas). El metano almacenado en estado licuado en cilindros instalados en el vehículo.
La exposición a la atmósfera
Ya hemos discutido el hecho de que el metano tiene un impacto sobre el efecto invernadero. Si el grado de la acción de monóxido de carbono (4) en el clima convencionalmente tomada como unidad, entonces 'gas de los pantanos' que la fracción es de 23 unidades. Durante los últimos dos siglos, los científicos han observado un aumento en el contenido cuantitativo de metano en la atmósfera de la Tierra.
Actualmente, la cantidad aproximada de CH4 se estima en 1,8 partes por millón. A pesar de que esta cifra es 200 veces menos que la presencia de dióxido de carbono, hay una conversación entre los científicos sobre el posible riesgo de atrapar el calor emitido por el planeta.
Debido a la excelente calorífico 'Marsh gas' se utiliza no sólo como un material de alimentación en la realización de la síntesis química, sino también como fuente de energía.
Por ejemplo, el metano operar una variedad de calderas de gas, columnas, diseñados para sistemas de calefacción individual en viviendas particulares y casas rurales.
Tal opción de auto-calentamiento es muy beneficioso para los propietarios de viviendas, no relacionados con el accidente, que se realiza de forma sistemática en los sistemas de calefacción centralizada. Debido caldera de gas que operan en un determinado tipo de combustible, es suficiente para 15-20 minutos con el fin de calentar totalmente la casa de dos pisos.

conclusión
El metano, estructural y las fórmulas moleculares de los que se han dado anteriormente, una fuente natural de energía. Debido al hecho de que incluye sólo átomos de carbono e hidrógeno, los ecologistas reconocen la seguridad ambiental de la hidrocarburo saturado.
En condiciones estándar (temperatura del aire de 20 grados Celsius y una presión de 101.325 Pa) la sustancia es gaseoso, no tóxico, insoluble en agua.
En caso de que la temperatura del aire se baja a -161 grados, es metano comprimido que se utiliza ampliamente en la industria.
El metano tiene un impacto en la salud humana. No es una sustancia tóxica, pero es un gas sofocante. Hay límites incluso (MAC) en el contenido de sustancias químicas en la atmósfera.
Por ejemplo, trabajar en las minas se permiten sólo en los casos en que la cantidad no supera el metro cúbico a 300 miligramos. El análisis de las características de una estructura de la materia orgánica posible concluir que las similitudes en las propiedades químicas y físicas con todos los otros miembros de la clase de hidrocarburos (límite) saturados.
Hemos analizado la fórmula estructural, la estructura espacial de metano. serie homóloga que comienza "gas de los pantanos" tiene la fórmula CnH2n molecular general + 2.
















