La tabla periódica de Mendeleiev y la ley periódica
Durante el siglo XIX una fuerte reforma sufrido muchas áreas, incluyendo la química. Sistema Periódico Mendeleev, formulada en 1869, ha conducido a una comprensión común de la relación entre la posición de las sustancias simples en la tabla periódica, para establecer la relación entre la propiedad relativa masa y el elemento de valencia atómica.
química Domendeleevsky entre
Un poco antes, en el siglo XIX, numerosos intentos de sistematización de los elementos químicos. El químico alemán Johann Wolfgang Döbereiner pasó el primer trabajo serio sobre la sistematización en el campo de la química. Se determinó que una serie de sustancias similares en propiedades se pueden agrupar – tríada.
La inexactitud de las representaciones de la científico alemán
La esencia de la ley representada por Johann Wolfgang Döbereiner tríadas determina de modo que el peso atómico de una sustancia está cerca de la mitad de la suma (valor medio) de las masas atómicas de los dos últimos elementos de la tabla de tríadas. 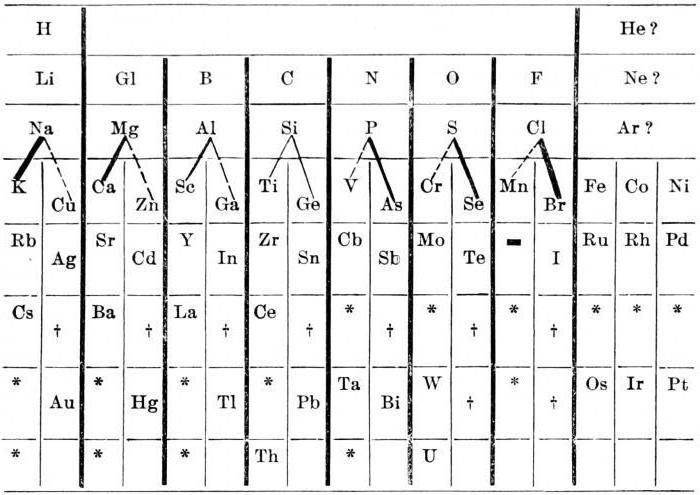 Sin embargo, la ausencia de magnesio en un único subgrupo de calcio, estroncio y bario era errónea.
Sin embargo, la ausencia de magnesio en un único subgrupo de calcio, estroncio y bario era errónea.
Este enfoque fue la consecuencia de las restricciones artificiales sustancias similares sólo triodidades. Johann Wolfgang Döbereiner podía ver las similitudes en los parámetros químicos de fósforo y arsénico, bismuto y antimonio. Sin embargo, se limitó Recuperando tríadas. Como resultado, no pudo llegar a la correcta clasificación de los elementos químicos.
En Elementos existentes, en Johann Wolfgang Döbereiner tríada, por supuesto, que no era posible, la ley indica claramente la presencia de la relación entre la masa atómica relativos propiedades y químicas de las sustancias simples.
elementos químicos proceso de sistematización
Todos los intentos posteriores de sistematizar confiaron en la distribución de los elementos en función de su masa atómica. Más tarde Johann Wolfgang Döbereiner hipótesis ha sido utilizado por otros químicos. Introducido formando tríadas, tétradas y pentadas (combinando en grupos de tres, cuatro y cinco elementos).
En la segunda mitad del siglo XIX hubo varios trabajos al mismo tiempo, en base al cual Dmitri Ivanovich Mendeleev química llevó a la sistematización completa de los elementos químicos. Diferente estructura de la tabla periódica llevó a una comprensión revolucionaria y la evidencia de una simple mecanismo de distribución de sustancias.
La tabla periódica de Mendeleiev de elementos
En una reunión de la Sociedad Química de Rusia en la primavera de 1869 se leyó un aviso en el científico ruso D. I. Mendeleeva sobre su descubrimiento de la ley periódica de los elementos químicos.  Al final del mismo año, la primera obra "Fundamentos de la Química", el primer sistema periódico de los elementos incluidos en ella se han publicado.
Al final del mismo año, la primera obra "Fundamentos de la Química", el primer sistema periódico de los elementos incluidos en ella se han publicado.
En noviembre de 1870, que mostró Además colegas, "sistema natural de los elementos y usarlo en la dirección de las cualidades de los elementos no descubiertos." En este trabajo I. D. Mendeleiev utilizó por primera vez el término "ley periódica". El sistema periódico de los elementos sobre la base de la ley periódica define la posible existencia de sustancias simples no abrir y indica claramente sus propiedades.
Correcciones y aclaraciones
Como resultado, en 1971 la ley periódica y el sistema periódico de elementos de Mendeleyev se han modificado y complementado por el químico ruso.
El artículo final "ley periódica de los elementos químicos" definición de conjunto científico de la ley periódica, que establece que las características de los cuerpos simples, las propiedades de los compuestos, y forman cuerpos complejos dependencia directa se determinan de acuerdo a su peso atómico.
Algo más tarde, en 1872, la estructura de la tabla periódica se ha reorganizado en una forma clásica (modo de período corto de distribución). 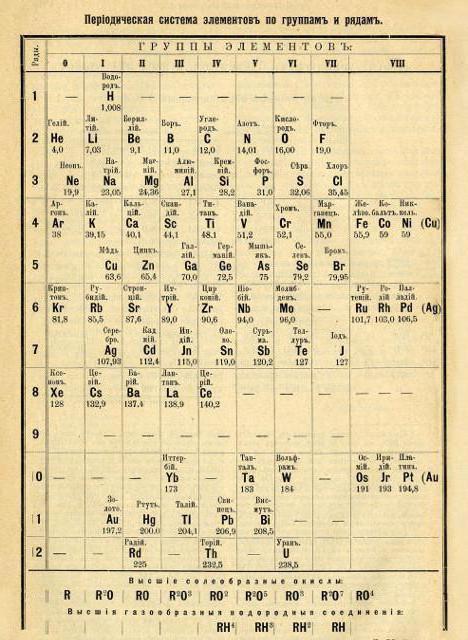
A diferencia de sus predecesores, el químico ruso hizo totalmente la mesa, introdujo el concepto de regularidad de los pesos atómicos de los elementos químicos.
Elementos característicos de la tabla periódica y leyes derivadas han permitido a los científicos describen las propiedades de los elementos aún por descubrir. Mendeleev se basó en el hecho de que las propiedades de cada sustancia se puede determinar de acuerdo con las características de los dos elementos adyacentes. Lo llamó la regla de las "estrellas". Su esencia es que los elementos químicos en la tabla para determinar las propiedades del elemento seleccionado necesario para ser guiado horizontal y verticalmente en una tabla de los elementos químicos.
periódica de Mendeleiev es capaz de predecir el …
Tabla de los elementos de Mendeleev, a pesar de su exactitud y fidelidad, no fue reconocido por la comunidad científica en su totalidad. Algunos de los grandes científicos de renombre mundial ridiculizado abiertamente la posibilidad de predecir las propiedades de los elementos no descubiertos. Fue sólo en 1885, después del descubrimiento de los elementos pronosticados – eka-aluminio, y ekabora ekasilitsiya (galio, escandio y germanio), un nuevo sistema de clasificación de la ley periódica de Mendeleev y han sido reconocidos como los fundamentos teóricos de la química.
A principios del siglo XX, la estructura de la tabla periódica corregido en varias ocasiones. En el proceso de obtener nuevos datos científicos D. I. Mendeleiev y su colega William Ramsay llegó a la conclusión de la necesidad de introducir un grupo cero. En su composición incluye gases nobles (helio, neón, argón, criptón, xenón y radón).
En mil novecientos once años Soddy hizo una propuesta para colocar elementos químicos indistinguibles – isótopos – en una sola celda de la tabla.
En el transcurso de un largo y laborioso trabajo de la tabla periódica de los elementos químicos de la tabla periódica se finalizó, y adquirió un aspecto moderno. Su estructura incluye ocho grupos y siete períodos. – grupos son períodos columnas verticales – horizontal. Los grupos definidos división en subgrupos. 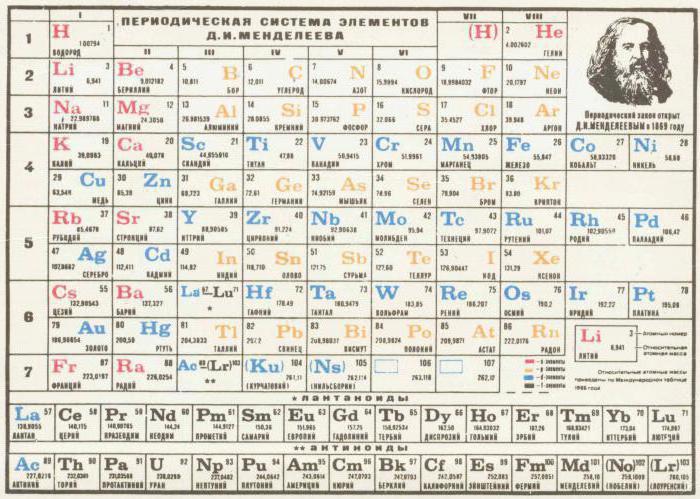
La posición en el elemento de la tabla indica sus electrones de valencia y las características puramente químicos. Al final resultó que, durante el desarrollo de la tabla periódica que se ha detectado una coincidencia el número de elementos del electrón con su número de serie.  Este hecho se simplifica aún más la comprensión del principio de la interacción de las sustancias simples y la formación de complejo. Un proceso como en dirección inversa. Calcular el número de este material, así como necesario para la reacción química era teóricamente disponible.
Este hecho se simplifica aún más la comprensión del principio de la interacción de las sustancias simples y la formación de complejo. Un proceso como en dirección inversa. Calcular el número de este material, así como necesario para la reacción química era teóricamente disponible.
El papel de los descubrimientos de la ciencia moderna de Mendeleev
sistema de Mendeleev y su enfoque a la ordenación de los elementos químicos determinan el desarrollo sensible de la química. Con la comprensión adecuada de la relación de las constantes y análisis químico Mendeleev podría montar correctamente y elementos agrupados según sus propiedades.  Nueva tabla de elementos hace que sea posible calcular con claridad y precisión los datos antes de la reacción química, la predicción de nuevos elementos y sus propiedades.
Nueva tabla de elementos hace que sea posible calcular con claridad y precisión los datos antes de la reacción química, la predicción de nuevos elementos y sus propiedades.
Apertura del científico ruso ha tenido un impacto directo en el curso ulterior del desarrollo de la ciencia y la tecnología. No hay un área tecnológica que no involucrada conocimiento de la química. Tal vez si tal descubrimiento no fue así, nuestra civilización se habría tomado un camino diferente de desarrollo.