compuestos complejos: nomenclatura y clasificación
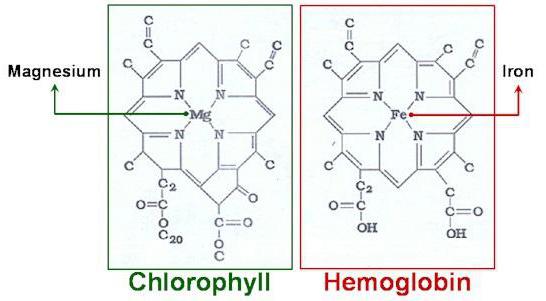
La mayor y más diversa entre los materiales inorgánicos es una clase de compuestos complejos. Para esto se puede atribuir al grupo de los compuestos organometálicos, tales como clorofila y hemoglobina. Es estas conexiones son el puente que conecta la química orgánica e inorgánica en una ciencia unificada. papel inestimable en el desarrollo de conocimientos materiales complejos en el campo de la química analítica y química del cristal, el estudio de los procesos biológicos más importantes: la fotosíntesis, interna (celular) respiración.
En este artículo vamos a examinar la estructura y nomenclatura de compuestos complejos, así como los principios básicos de su clasificación.
teoría Coordinación A. Werner
Al final del siglo XX científico suizo A. Werner demostró que la molécula en cualquier sustancia compleja varias estructuras que han sido respectivamente denominado el ion central, ligandos (ligandos) y la esfera de coordinación externa. Que estábamos clasificación y nomenclatura de compuestos complejos clara, explicamos estos conceptos con más detalle. Por lo tanto, A. Werner se ha demostrado en presencia de la molécula de iones (normalmente cargado positivamente), que ocupa una posición central. Se hizo conocido como el agente complejante, el ion central o átomo. Puede estar situado cerca de moléculas neutrales, llamados ligandos, y cargados negativamente partículas aniones que forman la esfera de coordinación interna del material. Todas las partículas restantes que no han entrado en él, forman la capa exterior de la molécula.
Por lo tanto, en la fórmula cuprite de sodio Na 2 [Cu (OH) 4], un átomo central de cobre en estado de oxidación +2 y cuatro gidroksogrupp constituye la esfera interior, mientras que los iones de sodio se encuentran a cierta distancia desde el átomo central en la esfera exterior.
Los métodos para determinar las fórmulas focales y los nombres de las sustancias
Hasta ahora, la teoría de A. Werner es la principal base teórica en la que estudia complejos complejos. Nomenclatura, es decir, los nombres de estas sustancias se determinan por las normas adoptadas por la Sociedad Internacional de Theoretical and Applied Chemistry.
Le damos varios ejemplos de fórmulas de sustancias, que contiene el átomo de complejos de platino – K 2 [PtCl 6] o moléculas NH 3 – [Ag (NH 3) 2] Cl. Al final resultó que, la fórmula puede ser derivada usando las siguientes prácticas: reacciones doble de cambio, la conductividad molar de soluciones método de difracción de rayos X. Tenga en cuenta estos métodos en detalle.
Como se muestra la estructura de compuestos de platino complejos
Sustancias de este grupo se caracterizan por la presencia en la molécula del átomo central de platino. Cuando el compuesto PtCl 4 × 6NH 3 acto solución de nitrato de plata, a continuación, todo el cloro presente en el material asociado con los átomos de metal y AgCl forma de copos blancos. Esto significa que todos los aniones son cloro en la esfera de coordinación externa, mientras que las moléculas de amoníaco estaban ligados al átomo central de platino y junto con él forman la esfera interior.
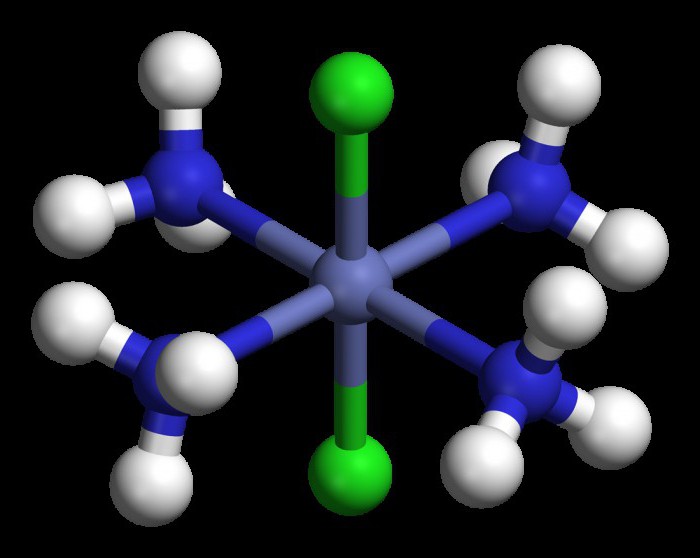
Esto significa un compuesto de coordinación de fórmula se registra en esta forma: [Pt (NH3) 6] Cl 4 y llamado cloruro de hexamina platino. Mediante el uso de método de difracción de rayos X, los químicos exploradas y otros compuestos complejos que nomenclatura se instalarán en la siguiente sección.
Los compuestos cristalinos de cromo
La estructura de este grupo de sustancias ha sido identificado por el proceso físico de difracción de rayos X del análisis de difracción de rayos X subyacente. Pasando a través de la red cristalina, la onda electromagnética dispersa por la acción de electrones de la sustancia de ensayo. Esto hace posible de forma muy precisa para determinar qué grupos de átomos se encuentran en los sitios de celosía. correspondiente nomenclatura de los compuestos complejos se ha creado a los cristales que contienen cromo. Ejemplos de nombres de hidratos isoméricas de sales de cromo trivalente, dibujado a través del método de difracción de rayos X, son los siguientes: cloruro de tetraakvadihlorohroma (III), cloruro de pentaakvahlorohroma (III).
Se encontró que en estos materiales átomo de cromo enlazado a seis ligandos diferentes. ¿Cómo se puede determinar la velocidad y cualquier factor que afecta el número de coordinación?
Como el átomo central está vinculada con ligandos
Para responder a las preguntas planteadas anteriormente, recordamos que en las inmediaciones del agente complejante son varias estructuras, llamados ligandos, o ligandos. Su número total, y determina el número de coordinación. Según la teoría de A. Werner, recepción, clasificación y nomenclatura de los compuestos complejos son directamente dependientes de este indicador. Se asocia correlativamente con la oxidación del átomo central. En los compuestos de platino, cromo, número de coordinación de hierro del máximo igual a seis; si el agente complejante se representa por átomos de cobre o zinc – cuatro si el átomo central es de plata o de cobre – dos.
Tipos de compuestos complejos
En química, que se distingue como las principales clases y categorías de las sustancias de transición entre ellas. Examen en los compuestos resúmenes complejos anteriores que nomenclatura indica la presencia en su estructura de moléculas de agua son aquacomplexes. Por amina incluir sustancias que contienen partículas neutras de amoníaco, tales como triyodo triamminrody. estructura molecular peculiar de la clase de compuestos quelantes. Su nombre proviene del término quelicera biológica – llamada garra decápodos. Estas sustancias contienen ligando, una configuración espacial que incluye un agente complejante, como garras. Tales compuestos incluyen complejo de oxalato férrico, complejo de platino etilendiamminovy con +4, sales de ácido aminoacético estado de oxidación, que contienen iones de rodio, platino o cobre.

Reglas para la compilación de los nombres de los compuestos complejos
La pregunta de la prueba más común en la búsqueda de la química en el curso de la escuela secundaria es: llamar el complejo compuesto de la IUPAC-nomenclatura. En un ejemplo específico, analizamos algoritmo compilar sustancia del título que tiene la siguiente fórmula: (NH4) 2 [Pt (OH) 2 Cl 4].
- Nombre comienza con la determinación de la composición de la esfera de coordinación interna. Contiene grupos hidroxilo y los aniones de cloro. Estos títulos se suman la terminación -o. Obtenemos digidrokso-, tetrahloro-.
- Ahora nos encontramos con el agente formador de complejos usando la notación su nombre en latín, y añadirá la AT sufijo entre paréntesis deberá indicar su grado de oxidación: platinato (IV).
- Acabado con símbolo de la esfera interior, mueva al exterior. Lo llamamos cación: en este ejemplo son los iones de amonio.
Como resultado, la sustancia tendrá un título en el que la totalidad de la estructura de la lista anterior.
El uso de compuestos de complejos
Al principio de este artículo llamamos a los representantes más importantes de sustancias organometálicos tales como la hemoglobina, clorofila, vitaminas. Ellos juegan un papel clave en el metabolismo. Ampliamente utilizado compuestos complejos en los ciclos tecnológicos de la fusión de metales ferrosos y no ferrosos. Un papel importante lo juega en carbonilos metalurgia – compuestos complejos específicos que nomenclatura indica la presencia en sus moléculas de CO monóxido de carbono como ligando. Estos compuestos se descomponen bajo calentamiento y la reducción de los metales tales como níquel, hierro, cobalto a partir de sus minerales. La mayoría de los complejos se utilizan también como catalizadores en las reacciones que producen los barnices, pinturas y plásticos.