El gas más pesado. El gas radón radiactivo: propiedades, características, vida media
Gas – uno de los estados de agregación de la sustancia. Los gases presentes en el aire, no sólo en la Tierra, pero en el espacio. Están asociados con facilidad, la volatilidad de la ingravidez. La más fácil es hidrógeno. Y lo que es el gas más pesado? Vamos a encontrar la misma.
Los gases más pesados
La palabra "gas" viene de la palabra griega "caos". Sus partículas son móviles y vagamente conectados entre sí. Se mueven al azar, llenando todo el espacio disponible. El gas puede ser un elemento simple y consiste de átomos de una sustancia y puede ser un compuesto de varios.

El gas pesado más simple (a temperatura ambiente) es el radón, su masa molar 222 g / mol. Él es radiactivo y es absolutamente incoloro. Después de que se considera el xenón más grave, una masa atómica de 131 g / mol. Los gases pesados restantes son compuestos.
Entre los compuestos inorgánicos del gas más pesado a una temperatura de 20 ° C es el fluoruro de tungsteno (VI). Su masa molar es 297,84 g / mol, y la densidad – 12,9 g / l. En condiciones normales, es un gas incoloro, fuma, y es de color azul en el aire húmedo. hexafluoruro de tungsteno es muy activo, que se convierte fácilmente en líquido cuando se enfría.
radón
Apertura de gas se produjo durante el período de estudio para el estudio de la radiactividad. Durante la desintegración de algunos elementos, los científicos han señalado reiteradamente alguna sustancia emitida con otras partículas. Rutherford llamó emanación.
Así se descubrió la emanación de torio – Torón, radio – radón, actinio – actinón. Más tarde se encontró que todas estas emanaciones son isótopos del mismo elemento – un gas inerte. Robert Gray y Uilyam Ramzay aislaron por primera vez en su forma pura e hicieron mediciones de sus propiedades.
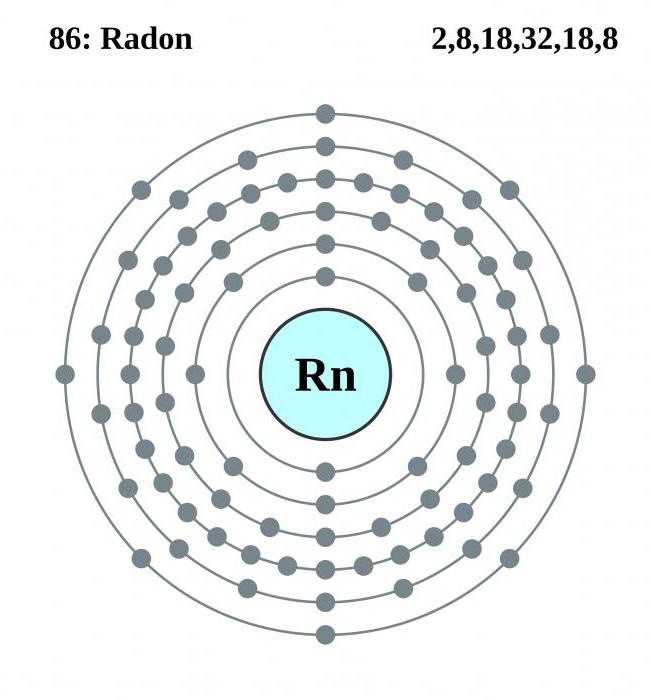
En el radón tabla periódica es un elemento del grupo 18 de número atómico 86. Se encuentra ubicado entre Francia y astato. En condiciones normales, la sustancia es un gas, no tiene sabor, olor y color.
Gas 7,5 veces más denso que el aire. Se disuelve en agua es mejor que los otros gases nobles. Los disolventes, esta cifra aumenta aún más. De todos los gases raros Él es el más activo, fácilmente interactuar con flúor y oxígeno.
El gas radón radiactivo
Una de las propiedades del elemento – la radiactividad. El elemento tiene treinta y cuatro isótopos naturales resto – artificial. Todos ellos son inestables y propensos a la desintegración radiactiva. La vida media del radón, más precisamente, su isótopo más estable, es de 3,8 días.
Debido a que el gas altamente radiactivo tiene fluorescencia. La sustancia gaseosa y líquida se pone de relieve en azul. El radón sólido cambia su paleta de amarillo a rojo cuando se enfrían a temperaturas de nitrógeno – sobre -160 ° C.
El radón puede ser muy tóxico para el hombre. pesados productos no volátiles tales como el polonio, plomo, bismuto resultante de su desintegración. Ellos están muy mal excretan. Sedimentación y acumular estas sustancias envenenan el cuerpo. Después de fumar, el radón es la segunda causa más común de cáncer de pulmón.
La ubicación y el uso de radón
El gas más pesado es uno de los elementos de tierras raras corteza. En la naturaleza, el radón es una parte de minerales que contienen uranio-238, torio-232, uranio-235. En su decadencia que se libera, caer en la atmósfera y la hidrosfera de la tierra.
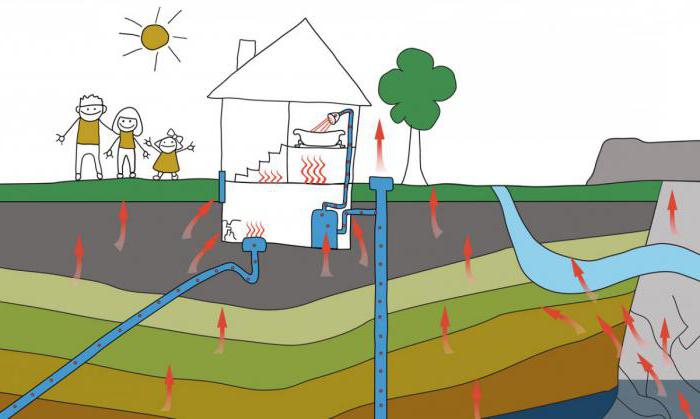
El radón se acumula en el río y las aguas del mar, las plantas y el suelo en materiales de construcción. En la atmósfera, su contenido aumenta como terremotos y actividad volcánica, la extracción de los fosfatos y las plantas de energía geotérmica.
Con la ayuda de este gas son las fallas tectónicas, depósitos de torio y uranio. Se utiliza en la agricultura para activar las mascotas de alimentación. El radón se utiliza en la metalurgia, el estudio de la hidrología subterránea, medicina baños de radón populares.